Kasvutekijäreseptoriperheen mysteerikuopus syövässä – ErbB4

Reseptorit ovat solukalvon läpäiseviä proteiineja, jotka välittävät solun ympäristöstä tulevia ulkopuolisia viestejä solun sisään, mikä aiheuttaa solussa vasteen. Käytännön esimerkki ovat aistimukset. Omassa tutkimuksessani keskityn solujen kasvuun, eloonjäämiseen ja liikkumiseen1,2 vaikuttavaan kasvutekijäreseptoriryhmän yhteen jäseneen, joka on ErbB4. Se kuuluu syövässä tunnettuun ErbB-reseptoriperheeseen, johon kuuluvat epidermaalinen kasvutekijäreseptori eli EGFR, ErbB2 ja ErbB3. Syöpätutkimuksessa näitä reseptoreja vastaan on pystytty kehittämään hoitokeinoja, vaikkakin paljon on vielä selvitettävänä, kuten lääkevastustuskyvyn synnyn estäminen.
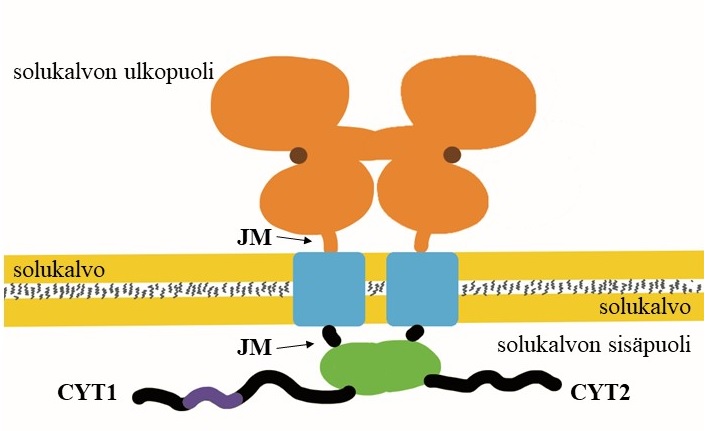
ErbB4 on siitä erityinen, että se koostuu neljästä alamuodosta, jotka vaikuttavat merkittävästi reseptorin toimintaan. Tutkimukseni tarkoitus on selvittää alamuotojen yhteisvaikutusta (ErbB4 JM-a CYT1 + JM-a CYT2, kuvassa) rintasyöpäkontekstissa. Aikaisemmissa reseptoritutkimuksissa alamuotoja on tutkittu erillään, koska niiden toimintaan on pyritty selvittämään. Tutkimukseni on luonnollinen jatkumo tälle, koska nyt on aika ymmärtää niiden yhteisvaikutus solun viestinvälityksessä, sillä luonnossa ErbB4-reseptorin alamuodot ilmenevät yhdessä3 ja pariutuvat yhdeksi toimivaksi ErbB4-reseptoriksi.
On tärkeää tuoda tämä näkökulma ErbB4-reseptorin tutkimukseen, sillä joissain tutkimuksissa on yleisesti käsitelty ErbB4-reseptoria ilman varsinaista mainintaa alamuodoista, vaikka niiden tiedetään toiminnallisesti eroavan toisistansa. Syöpätutkimuksissa on lisäksi ristiriitaisuutta ErbB4-toiminnasta: 1) mikä reseptorin alamuodoista aiheuttaa syöpää, 2) estääkö ErbB4-reseptori syövän kehitystä joissain syövissä. Tämä luo myös viimeisen tärkeän osa-alueen tutkimukseeni. Ovatko yleisesti käytössä olevat muita ErbB-reseptoreja vastaan kehitetyt lääkkeet toimiva lähestymistapa ErbB4-reseptoria vastaan syövässä, kun molemmat alamuodot CYT1 ja CYT2 ilmenevät syöpäsoluissa4?
Lopuksi vielä miten ErbB4-reseptorin alamuodot eroavat toisistansa? ErbB4-reseptorin alamuodot eroavat solukalvon rajapinnoilta JM-a- ja JM-b-alamuodoksi, joista ainoastaan JM-a-alamuoto pystyy viestimään reseptorin sisäpuolisen toiminnallisen osan vapauttamisella solulimaan5,6. Toinen alamuotojen jakoperuste tapahtuu solun sisäpuolisen toiminnallisen osan ”hännän” perusteella CYT1- ja CYT2-alamuodoksi. CYT1-alamuoto sisältää sitoutumiskohdat solun kasvua ja jakaantumista edistävän mutta myös hajotuksen aikaansaavien proteiinien kiinnittymiseen. Kyseinen ominaisuus puuttuu ErbB4-reseptorin CYT2-alamuodolta7,8.
Fred Saarinen
Kirjoittaja on Turun molekyylilääketieteen tohtoriohjelman (TUdMM) kolmatta vuotta aloittava jatko-opiskelija.
Lähteet
- Ullrich, A. & Schlessinger, J. Signal transduction by receptors with tyrosine kinase activity. Cell 61, 203–212 (1990).
- Blume-Jensen, P. & Hunter, T. Oncogenic kinase signalling. Nature 411, 355–365 (2001).
- Machleidt, A. ja muut. The prognostic value of her4 receptor isoform expression in triple-negative and her2 positive breast cancer patients. BMC Cancer 13, 1–10 (2013).
- Paatero I. & Elenius K. ErbB4 and its isoforms: patentable drug targets? Recent Pat DNA Gene Seq. 2, 27–33 (2008).
- Ni, C.-Y. ja muut. gamma -secretase cleavage and nuclear localization of ErbB-4 receptor tyrosine kinase. Science 294, 2179–2181 (2001).
- Rio, C. ja muut. Tumor necrosis factor- alpha -converting enzyme is required for cleavage of erbB4 / HER4. J. Biol. Chem. 275, 10379–10387 (2000).
- Junttila, T. T. ja muut. Identification of patients with transitional cell carcinoma of the bladder overexpressing ErbB2, ErbB3, or specific ErbB4 isoforms: real-time reverse transcription-PCR analysis in estimation of ErbB receptor status from cancer patients. Clin. Cancer Res. 9, 5346–5357 (2003).
- Sundvall, M. ja muut. Isoform-specific monoubiquitination, endocytosis, and degradation of alternatively spliced ErbB4 isoforms. Proc. Natl. Acad. Sci. U. S. A. 105, 4162–7 (2008).